Specialista in Diagnostica per Immagini: RX, Ecografie, TC, RM, Mammografie
Ricevere un referto, sentire parlare di “familiarità” o leggere la parola BRCA può accendere subito l’ansia: “E se fosse genetico? E se toccasse anche a mia sorella, mia figlia, mia madre?”. È una reazione normale.
La buona notizia è che oggi abbiamo strumenti molto solidi per stimare il rischio, fare prevenzione personalizzata e — quando serve — arrivare a una diagnosi precoce, spesso in fase curabile. E tutto inizia dal capire bene cosa significano BRCA1 e BRCA2 e quando ha senso chiedere un counseling genetico.
Cos’è BRCA1 e BRCA2 e cosa vuol dire “tumore ereditario”
BRCA1 e BRCA2 sono geni “oncosoppressori”: aiutano le cellule a riparare il DNA quando si danneggia. Se una persona nasce con una variante patogenetica (spesso detta “mutazione”) in uno di questi geni, la capacità di riparazione si riduce e aumenta la probabilità di sviluppare alcuni tumori, soprattutto mammella e ovaio, ma anche pancreas e (in particolare per BRCA2) prostata.
È fondamentale però una frase: aumenta il rischio non significa certezza. Non tutte le persone portatrici si ammaleranno.
Familiare, ereditario, sporadico: differenze
- Sporadico: il tumore “capita” senza un’alterazione ereditaria riconoscibile; è la situazione più frequente.
- Familiare: in una famiglia ci sono più casi, ma non necessariamente c’è una mutazione identificabile (possono contare anche fattori condivisi e la statistica).
- Ereditario (genetico): c’è una variante patogenetica trasmessa in famiglia (BRCA o altri geni). In questo caso il rischio è più alto e la prevenzione cambia.
In Italia, una quota circa 5–10% dei tumori della mammella è considerata ereditaria.
“Parole da referto” che confondono spesso (e cosa significano davvero)
Questi termini non sono “sentenze”: sono un modo standardizzato per descrivere ciò che si vede.
- BI-RADS: scala (0–6) che indica il livello di sospetto e cosa fare dopo.
- BI-RADS 1–2: negativo/benigno
- BI-RADS 3: probabilmente benigno → controllo ravvicinato
- BI-RADS 4–5: sospetto/altamente sospetto → in genere biopsia mirata
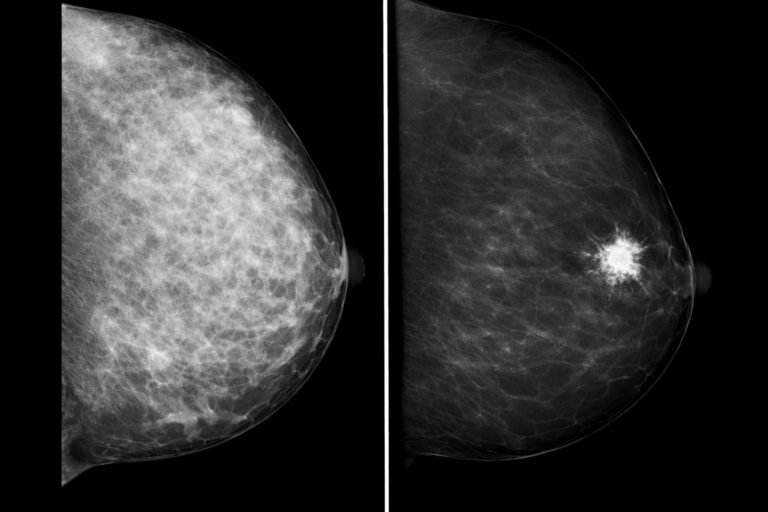
- Densità mammaria (seno “denso”): tanto tessuto ghiandolare; può rendere la mammografia meno “trasparente” e aumentare il valore di ecografia e RM in contesti selezionati.
- Ipoecogeno (eco): area più “scura” rispetto al tessuto intorno; è un descrittore, non una diagnosi.
- Margini spiculati / irregolari: contorni “a raggi” o non netti; aumentano il sospetto, soprattutto se associati ad altri segni.
- Microcalcificazioni (mammografia): piccoli depositi di calcio; alcune morfologie/distribuzioni richiedono approfondimento.
- Enhancement (RM con contrasto): quanto una zona “capta” il mezzo di contrasto; pattern e cinetica aiutano a distinguere benigno/sospetto (ma non sono infallibili).
Qui entra in gioco la radiologia “di qualità”: non è solo vedere un’immagine, è contestualizzarla (età, rischio, storia clinica) e scegliere il percorso corretto.
Perché è importante conoscere lo stato BRCA
“Se ho una mutazione BRCA, cosa cambia?”
Risposta diretta: cambia il programma di prevenzione, spesso più precoce e più intenso (per esempio con RM annualein età giovane), e in alcuni casi cambiano anche le opzioni di riduzione del rischio e le scelte terapeutiche se una diagnosi è già presente.
“Avere parenti con tumore al seno significa che ho BRCA?”
Risposta diretta: no. La familiarità aumenta il sospetto, ma serve una valutazione strutturata (albero genealogico, età di diagnosi, tipi di tumore). Il passo giusto è il counseling genetico, non un test “fai da te”.
“BRCA aumenta tanto il rischio?”
Risposta diretta: sì, in media il rischio di tumore al seno può arrivare a coinvolgere 5–7 donne su 10 portatrici nel corso della vita (stime variabili tra studi). Anche il rischio ovarico, soprattutto per BRCA1, aumenta in modo importante.
Quando sospettare una forma ereditaria e chiedere il counseling genetico
La regola pratica è: pochi casi non bastano, ma alcuni segnali “pesano” molto.
Secondo raccomandazioni italiane (AIOM), sono indicazioni tipiche all’invio a consulenza genetica situazioni come:
- Tumore della mammella nell’uomo
- Tumore al seno in donna <36 anni
- Tumore al seno triplo negativo (un sottotipo biologico) in età <60 anni
- Tumore al seno bilaterale in età giovane (es. <50 anni)
- Tumore ovarico epiteliale non mucinoso (a qualsiasi età)
- Combinazioni “familiari” di tumore al seno/ovaio/pancreas/prostata metastatica in parenti di primo grado (e, per il lato paterno, anche alcuni parenti di secondo grado).
Un punto importante: anche le linee guida internazionali suggeriscono di valutare il rischio con strumenti rapidi quando c’è storia personale o familiare compatibile e, se positivo, inviare a counseling e test.
E le differenze cliniche tra ereditario e non ereditario?
In media, le forme ereditarie tendono più spesso a:
- comparire più precocemente,
- presentare più tumori primitivi nella stessa persona (es. bilateralità),
- avere associazioni tipiche (es. BRCA1 più spesso legato a fenotipi triplo negativi/basal-like).
Sono tendenze: non sostituiscono mai la valutazione genetica.
Come funziona in pratica: percorso del paziente (dalla richiesta al follow-up)
- Valutazione del rischio (medico curante / senologo / ginecologo / oncologo): si ricostruisce la storia personale e familiare e si decide se inviare al counseling.
- Counseling genetico: qui si chiarisce cosa può dire il test, cosa non può dire, implicazioni per familiari, possibili esiti (positivo/negativo/incerto). L’ISS sottolinea la necessità di un percorso con genetista esperto e consenso informato.
- Test genetico (di solito su sangue o saliva): oggi spesso si usa un pannello che include BRCA e altri geni, a seconda del caso.
- Interpretazione del risultato
- Variante patogenetica: si attiva un piano di prevenzione/riduzione rischio per la persona e si valuta il test predittivo nei familiari.
- Negativo: non significa “rischio zero”, ma si ricalibra il rischio sulla storia familiare.
- VUS (variante di significato incerto): non guida decisioni drastiche; si segue il rischio clinico.
- Sorveglianza e prevenzione personalizzataNelle donne ad alto rischio (es. BRCA), molte società scientifiche raccomandano RM mammaria annuale a partire da età giovane (circa 25–30 anni, a seconda del profilo), spesso affiancata nel tempo da mammografia secondo protocolli.
Benefici e limiti
Benefici
- Maggiore probabilità di diagnosi precoce, soprattutto con RM nei contesti ad alto rischio.
- Percorsi più mirati: meno “fai un controllo ogni tanto”, più “questo è il tuo piano”.
- Informazioni utili anche per i familiari (prevenzione mirata).
Limiti e rischi
- Falsi positivi: più controlli = più probabilità di trovare cose che poi si rivelano benigne → ansia e talvolta biopsie inutili.
- Falsi negativi: nessun esame è perfetto.
- Radiazioni: la mammografia usa dosi basse, ma nei percorsi ad altissimo rischio e in età molto giovane si privilegiano strategie che limitano l’esposizione, quando appropriato.
- Aspetto psicologico/familiare: sapere di essere portatori può pesare; per questo il counseling è parte della cura, non burocrazia.
Il ruolo del radiologo senologo
Nelle forme ereditarie, la differenza la fa l’esperienza del team — e il radiologo è centrale perché:
- sceglie l’esame giusto per età e rischio (non esiste un “sempre RM” o “sempre eco”);
- interpreta con criteri standard e riduce la variabilità;
- coordina gli approfondimenti: second-look ecografico, biopsie ecoguidate/stereotassiche/RM-guidate quando necessarie;
- integra imaging e clinica in un percorso che punta a diagnosi precoce, ma anche a evitare esami inutili.
In pratica: l’obiettivo non è “fare più esami”, è fare quelli giusti, al momento giusto.
FAQ – Domande frequenti
BRCA si eredita da madre o da padre?
Da entrambi: conta la linea materna e paterna.
Se il test BRCA è negativo, posso stare tranquilla?
Riduce la probabilità di una predisposizione BRCA, ma il rischio complessivo va ricalcolato su storia familiare e altri fattori.
La RM mammaria è “meglio” della mammografia?
Non in assoluto: è più sensibile in alcune fasce ad alto rischio, ma può dare più falsi positivi. La scelta dipende dal profilo di rischio.
Conclusioni
Parlare di BRCA1 e BRCA2 non significa vivere nell’ansia: significa usare informazioni potenti per fare prevenzione “su misura”. Se nella tua storia (personale o familiare) ci sono segnali compatibili, il passo più corretto è chiedere un counseling genetico: ti aiuta a capire se il test serve davvero e, soprattutto, cosa fare dopo.
Messaggio finale: con i percorsi giusti, la diagnosi precoce diventa un obiettivo concreto. E quando hai dubbi su un referto o su quale esame scegliere, confrontarti con un team esperto di senologia (radiologo incluso) può fare la differenza.
Riferimenti essenziali
- Associazione Italiana di Oncologia Medica (AIOM) – Raccomandazioni per implementazione test BRCA (2021).
- ISSalute (Istituto Superiore di Sanità) – “BRCA1 e BRCA2: quando farla” (agg. 02/04/2025).
- Fondazione AIRC – Mutazioni BRCA1/2 e rischio (14/11/2024).
- USPSTF – BRCA-related cancer: risk assessment, genetic counseling and testing (2019).
- EUSOBI – Indicazioni generali su RM in donne ad alto rischio/BRCA (pagina pazienti).
- NCCN Guidelines / Insights su valutazione genetica ereditaria (overview/insights).
- Review fenotipo BRCA1 e associazione con triplo negativo/basal-like.